2024.04.24-26 동안 KINTEX 에서 '제약/바이오' 포함 포장, 물류, 화장품, 화학/제품/기기 관련 다양한 행사 (ICPI WEEK 2024)가 있었는데요. DI 관련해 진행된 세미나 내용 Summary를 공유 합니다.

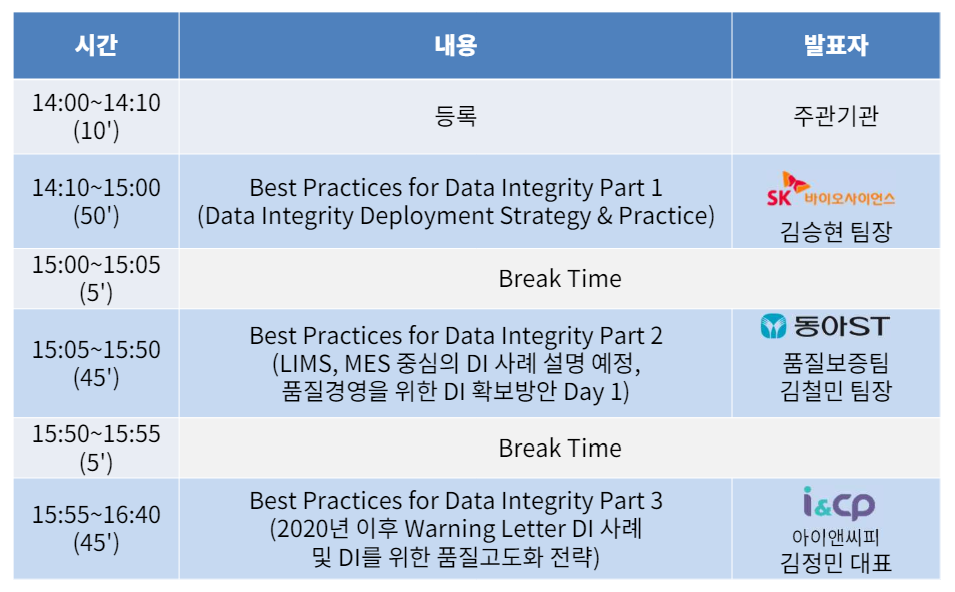
SK 바이오사이언스 QA 팀장님께서 서두 말씀하셨던 Risk based approach - Lifecycle - CAPA 의 중요성에 대해서 공감이 되었고, 동아ST 에서 공유해 주신 구체적 운영 사례들이 흥미로웠습니다. 아래 내용은 강연 내용을 summary 한 것입니다. AI Tool 로 summary 한 점 참고 하시면 좋겠습니다. (AI 정리 Tool 은 릴리스AI 활용해 보셔도 좋습니다)

1. 데이터 완전성 (Data Integrity)의 중요성과 그 역할
1-1. 데이터 완전성 정의와 중요성
- 데이터는 제품 품질의 완전성을 보증하는 근본적인 뒷받침 역할을 함
- (중요) 데이터 완전성 유무가 회사의 브랜드 이미지와 생존에 결정적임
- 데이터 완전성 불량은 제품 안전성에 직접적인 영향을 미치며, 실사 중 지적 사항을 받는 것을 방지함
1-2. 데이터 완전성 구성요소 및 그 역할
- 데이터 완전성을 위조하거나 의도적으로 변조하는 행위가 대상임
- (중요) 데이터 완전성을 구성하는 요소는 시스템과 절차에 의존적임
- 각자의 역할을 다하지 않으면 데이터 완전성을 보장할 수 없음
1-3. 실제 상황에서 데이터 완전성의 적용
- 모든 작업자는 방법성과 절차를 따르되, 실수는 인간의 한계로 인함
- 직원들에게 근거 없는 신뢰를 주는 행위는 직무유기로 간주됨
- (중요) 데이터 완전성을 확보하기 위해선 각자의 역할을 다해야 함

2. 데이터 완전성 문제와 해결
2-1. 데이터 완전성 문제점과 원인 이해
- (중요) 데이터 완전성, 즉 데이터 통합성은 데이터의 정확성과 일관성을 보장하는 것을 의미함
- GMP를 관리하는 사람들이 기본적으로 데이터 완전성을 준수해야 하며, 그렇지 않을 경우 제재를 받을 수 있음
- 실사 기관인 FDA나 유럽 등에서도 데이터 완전성을 강조하고 있음
- 데이터 완전성 위반은 주로 작업자의 오류로 인해 발생함
2-2. 데이터 완전성의 근본적 해결 방법
- 근본적인 데이터 완전성 문제의 해결은 작업자의 교육에 있음
- 교육은 카파를 하기 위한 중요한 단계이나, 실제로는 카파에 필수적인 교육보다는 그 반대의 역할을 하는 경우가 많음
- 교육이 모든 것을 해결하는 방법이 아니라, 제대로 된 교육을 통해 근본 원인을 찾아내야 함
- 교육이 아무리 중요한 기능이지만, 실제로는 교육만으로 모든 것을 해결하려 하지 않도록 주의가 필요함
2-3. 실사 및 가이드라인을 통한 데이터 완전성 관리
- (중요) 실사 결과에 따라 회사에 처벌이나 금지 조치가 이루어질 수 있음
- FDA는 매니지먼트 리스크와 제품 판매 수익에 대한 데이터 인테그리티의 중요성을 강조함
- 데이터 인테그리티 문제의 근본적인 해결을 위해, 가이드라인을 준수하고, 실사를 받아야 함
- 유럽은 데이터 인테그리티의 근본 원인을 잘못 찾아내는 것이 아니라, 근본 원인을 찾아 원인과 해결책을 찾는 것을 중요시함
3. 데이터 인테그리티 관리 전략
3-1. 데이터 완전성의 중요성과 관리 전략
- (중요) 데이터 완전성은 없던 개념이 아니며 동일 이슈로 묶여 강조된 것일 뿐임 이는 CCS 규정 도입에서도 마찬가지 이며 새로운 개념의 도입이 아닌 기존 프로세스 전반에서 오염 관리 중요 포인트 및 규정 관점에서 묶인 개념임
- 제품을 만드는 원자재에서부터 제품이 만들어질 때까지의 절차 관리가 중요함
- 데이터 인테그리티 관리는 단순히 기술적인 부분이 아니라 사람과 문화까지 포함
- 잘못된 습관은 큰일과 사람의 생명을 위협할 수 있음
- 올바른 데이터 완전성 관리를 위해서는 끊임없는 모니터링과 관리가 필요함
3-2. 데이터 완전성 실천을 위한 관리 전략
- (중요) 데이터 완전성 실천을 위해서는 시스템 운영 절차를 Specific 하고 Clear하게 만드는 것이 중요함
- 오류를 줄이는 것이 중요하며, 이는 시스템 운영 절차를 효율적으로 만드는 것과 연관 있음
- 관리 전략을 구체적으로 실천하기 위해서는 키 딜리버블스와 키 팩터들을 정확하게 설정해야 함
- 이러한 관리 전략을 만드는 것은 단순히 1명의 업무자가 할 수 있는 일이 아님
3-3. 데이터 인테그리티 실천을 위한 팀 작업
- 데이터 인테그리티를 관리하기 위해선 팀 작업이 필요함
- 프로젝트 팀을 꾸리고, 그 팀이 가지는 목적을 정하고, 그 목표를 달성하기 위해서 일을 하는 것이 필요함
- (중요) 이는 매우 어렵고 오랜 시간이 필요하며, 잘 시작되더라도 계속적인 관리와 모니터링이 필요함
- 데이터 인테그리티 실천을 위해 팀원들의 역량 개발도 중요함
- 이를 통해 끊임없는 개선과 혁신을 도모하여 데이터 인테그리티를 높여가는 것이 중요함

4. 데이터 거버넌스 시스템의 중요성 및 관리
4-1. 데이터 거버넌스 시스템의 정의 및 필요성
- 데이터는 의사결정의 기본이 됨
- (중요) 데이터 거버넌스 시스템은 데이터의 생명주기 관리를 의미함
- 데이터 인테그리티, SOP, 다큐멘테이션 등에 대한 관리가 필요함
- 제조업체의 목표는 각 기기에 따른 규정을 지키며 사용할 수 있게 하는 것임
- Computerized system (컴퓨터화 시스템) 사용시 CFR 11 규정에 따른 평가에 따라 (ES/ER 사용 여부) 강제성이 없었으나, DI 규정에서는 데이터 완전성 근거 기반하에 반드시 요구되는 기준 사항임
4-2. 데이터 거버넌스의 여러 측면
- 기기와 원료에 대한 오디트레일이 중요함
- (중요) 데이터의 중요성에 따라 관리 기준을 타이트하게 하는 것이 필요함
- 컴퓨터 시스템의 중요성과 이를 사용하는 것에 대해 강조함
- 중요 프로세스 및 데이터 생성/처리가 필요한 공정에서 컴퓨터를 사용하지 않는 경우, 시스템 변경이 필요함
4-3. 데이터 거버넌스 시스템의 구성
- 강사는 데이터 거버넌스의 중요성과 컨텐츠에 대해 설명함
- 시스템을 구성하는 구성 요소에는 EMS, WMS 등의 다양한 전자시스템이 있음
- 시스템을 사용하는 경우, 품질관리 및 제품 품질 향상에 도움이 됨
- (중요) 시스템이 제대로 작동하면 FDA clearance를 얻을 수 있음
- 올바른 시스템의 사용으로 데이터의 오류를 줄이고, 정확한 의사결정을 할 수 있음
5. 데이터 완전성 및 개선 방안에 대한 강의
5-1. 데이터 완전성 개념 및 필요성
- (중요) 데이터 완전성이란 데이터 내 생산, 저장, 전송 등 과정에서의 일관성을 말함
- 데이터 완전성은 중요한 정보의 유실이나 변경을 방지하며, 불필요한 비용을 절감함
- 서약서를 통해 데이터 완전성의 제도화 중요성을 강조함
- 데이터 완전성을 통해 동일한 데이터 세트에 대해 일관된 분석을 가능하게 함
5-2. 데이터 완전성 홍보 부스 개최 및 실행
- (중요) 데이터 완전성 홍보 부스를 개최하여 자신들의 수준을 시사함 (D웅제약 캠페인 사례)
- 설문을 통해 부스에 방문한 사람들의 반응을 듣고, 그에 따라 행동 개선 방향을 결정함
- 부스를 통해 일부분만 개선하기보다는 전체적인 데이터 인테그리티를 향상시키려고 노력함
- 각 개인이 개선해야하는 부분과 필요한 조치를 알림
5-3. 데이터 완전성 개선을 위한 방안
- (중요) 데이터 인테그리티를 개선하기 위해서는 리스크 베이스 어프로치가 필요함
- 현재의 문제를 단편적으로 해결하려 하지 않고, 데이터 인테그리티의 전반적인 개선을 위해 카파를 이용함
- 문제의 원인을 파악하고, 그 원인을 개선하기 위해 필요한 부분을 찾아내어 개선함
- 주최 측의 동참을 통해 전체적인 데이터 인테그리티 개선에 기여함
*강연 파일 PDF
'데이터 완전성 (Data Integrity)' 카테고리의 다른 글
| CSA, Computer Software Assurance FDA 지침 초안 번역 (0) | 2024.05.31 |
|---|---|
| 동아ST DI 강연 summary (킨텍스 세미나) (0) | 2024.05.08 |
| Audit trail 기능이 없는 장비, 기기, 시스템 처리 방법 (0) | 2024.04.23 |
| QC 실험실 시간 관리 (시간 동기화) (2) | 2024.04.12 |
| Windows 환경의 Data Integrity + Windows event viewer (2) | 2024.02.20 |




댓글